Hướng dẫn giải Câu hỏi trang 41 Luyện tập Bài 6. Giới thiệu về liên kết hóa học SGK Khoa học tự nhiên 7 Chân trời sáng tạo. Gợi ý: Nguyên tử Cl có 7 electron lớp ngoài cùng =>.
Câu hỏi/Đề bài:
|
Vẽ sơ đồ hình thành liên kết cộng hóa trị trong các phân tử sau: |
Hướng dẫn:
– Nguyên tử Cl có 7 electron lớp ngoài cùng => Cần nhận thêm 1 electron
=> Bỏ ra 1 electron để góp chung
– Nguyên tử H và nguyên tử N đều là phi kim
+ Nguyên tử H có 1 electron ở lớp ngoài cùng => Cần nhận thêm 1 electron
+ Nguyên tử N có 5 electron ở lớp ngoài cùng => Cần nhận thêm 3 electron
Lời giải:
– Xét phân tử khí chlorine
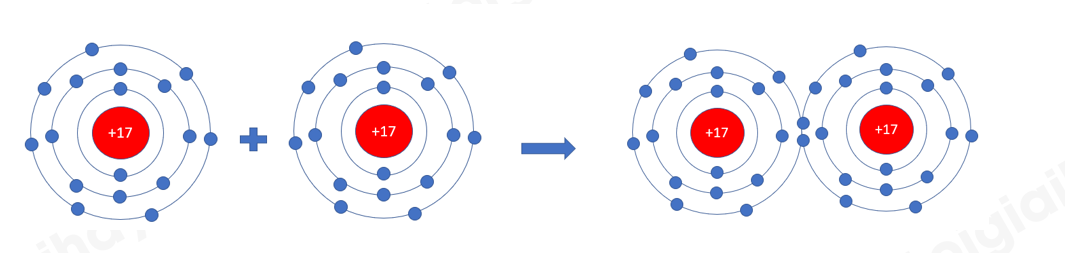
=> Mỗi nguyên tử Cl có 7 electron ở lớp ngoài cùng. Để có cấu trúc electron bền vững của khí hiếm Ar, khi hình thành phân tử chlorine, hai nguyên tử Cl đã liên kết với nhau bằng cách mỗi nguyên tử Cl góp chung 1 electron tạo thành 1 cặp electron dùng chung
– Xét phân tử khí amonia
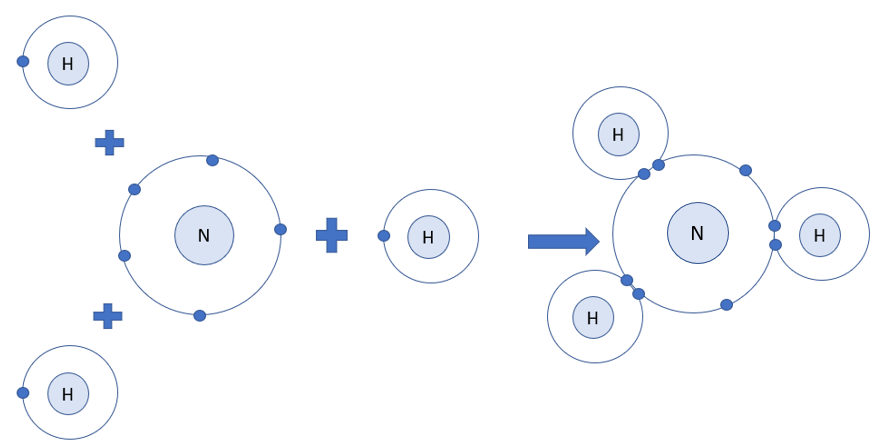
– Nguyên tử H có 1 electron ở lớp ngoài cùng
– Nguyên tử N có 5 electron ở lớp ngoài cùng
=> Nguyên tử H cần thêm 1 electron và N cần thêm 3 electron để đạt cấu hình electron bền vững của khí hiếm
=> Khi 3 nguyên tử H và 1 nguyên tử N liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử N góp ra 3 electron để tạo ra 3 đôi electron dùng chung