Hướng dẫn giải Câu hỏi Hoạt động trang 132 SGK Hóa 12 Kết nối tri thức – Bài 27. Đại cương về kim loại chuyển tiếp dãy thứ nhất. Hướng dẫn: Từ thể tích dung dịch KMnO4 đã dùng, xác định nồng độ Fe2+ trong dung dịch đã pha.
Câu hỏi/Đề bài:
Thí nghiệm: Xác định hàm lượng muối Fe(ll) bằng dung dịch thuốc tím
– Chuẩn bị:
+ Hoá chất: các dung dịch: KMnO4 0,02 M, H2SO4 10%, FeSO4 có nồng độ khoảng 0,10 M.
+ Dụng cụ: pipette 5 mL, burette 25 mL, bình tam giác 100 mL, ống đong 10 mL, bình tia nước cắt, giá đỡ, kẹp càng cua.
– Tiến hành:
+ Dùng pipette lấy 5,0 mL dung dịch FeSO4 cho vào bình tam giác; thêm tiếp khoảng 5 mL dung dịch H2SO4 10% (lấy bằng ống đong).
+ Cho dung dịch KMnO4 vào burette, điều chỉnh thể tích dung dịch trong burette về mức 0.
+ Mở khoá burette, nhỏ từng giọt dung dịch KMnO4 xuống bình tam giác, lắc đều. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mắt màu.
+ Tiếp tục chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dùng chuẩn độ.
– Ghi lại thể tích dung dịch KMnO4 đã dùng. Tiến hành chuẩn độ 3 lần, ghi số liệu vào vở và xử lí số liệu theo mẫu bảng sau:
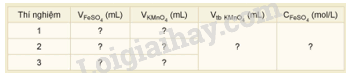
Lưu ý: Trong quá trình chuẩn độ, ban đầu thuốc tim mắt màu chậm, sau đó mắt màu nhanh.
Hướng dẫn:
Từ thể tích dung dịch KMnO4 đã dùng, xác định nồng độ Fe2+ trong dung dịch đã pha.
Lời giải:
Giả sử thể tích dung dịch KMnO4 trong thí nghiệm đã dùng là V (L).
=> \({{\rm{n}}_{{\rm{KMn}}{{\rm{O}}_{\rm{4}}}}} = 0,02{\rm{V (mol)}}\)
Theo phương trình hóa học: \({{\rm{n}}_{{\rm{F}}{{\rm{e}}^{{\rm{2 + }}}}}}{\rm{ = 5}}{{\rm{n}}_{{\rm{KMn}}{{\rm{O}}_{\rm{4}}}}} = 0,1{\rm{V (mol)}}\)
\( \Rightarrow {{\rm{C}}_M}{\rm{(F}}{{\rm{e}}^{2 + }}{\rm{) = }}\frac{{0,1{\rm{V}}}}{{0,01}}{\rm{ (M)}}\)