Đáp án Câu 19.23 Bài 19. Carboxylic acid (trang 96, 97, 98, 99, 100, 101) – SBT Hóa 11 Chân trời sáng tạo. Hướng dẫn: Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid.
Câu hỏi/Đề bài:
Ethyl acetate là chất lỏng, có mùi đặc trưng, được sản xuất ở quy mô lớn làm dung môi trong công nghiệp.
a) Viết phương trình hoá học điều chế ethyl acetate bằng cách đun nóng hỗn hợp acetic acid với ethanol, xúc tác H2SO4 đặc.
b) Sơ đồ thí nghiệm sau mô tả quá trình thực hiện phản ứng trên. Hãy cho biết vai trò của cốc nước lạnh trong thí nghiệm. Sau khi kết thúc phản ứng, ta thêm một ít nước vào ống nghiệm, lắc nhẹ thì có hiện tượng gì xảy ra?
c) Để một nhà máy sản xuất được 1.000 L ethyl acetate mỗi ngày thì lượng thể tích (L) ethanol và acetic acid tiêu thụ tối thiểu là bao nhiêu? Biết rằng hao hụt trong quá trình sản xuất trên là 34%.
Cho khối lượng riêng (g/cm3) của ethyl acetate, ethanol và acetic acid lần lượt là: 0,902; 0,79; 1,049.
Hướng dẫn:
a) Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid.
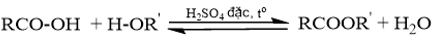
b) Ethyl acetate mới tạo thành tồn tại ở dạng hơi.
Ester không tan trong nước, nhẹ hơn nước, có mùi thơm đặc trưng.
c) Tính hiệu suất của phản ứng.
Tính số mol của ethylacetate rồi suy ra số mol và khối lượng của ethanol và acetic acid.
Sử dụng công thức: \[{\rm{V = }}\frac{{\rm{m}}}{{\rm{D}}}\]. Từ đó tính thể tích ethanol và acetic acid thực tế tiêu thụ.
Lời giải:
a) Phương trình hoá học điều chế ethyl acetate:
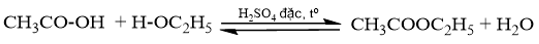
b) Vai trò của cốc nước lạnh: ethyl acetate sinh ra dưới dạng hơi nên cần làm lạnh bằng nước đá để hơi ethyl acetate ngưng tụ.
Hiện tượng: Sau khi kết thúc phản ứng, ta thêm một ít nước vào ống nghiệm, lắc nhẹ thì dung dịch không màu trong ống nghiệm tách lớp, có mùi đặc trưng.
c) Ta có: \[{{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}}} = 1000 \times 1000 \times 0,902 = 902000{\rm{ (g)}}\]
\[ \Rightarrow {{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}}} = \frac{{902000}}{{88}} = 10250{\rm{ (mol)}}\]