Lời giải Câu hỏi trang 110 Hoạt động Bài 21. Nhóm halogen SGK Hóa 10 Kết nối tri thức. Tham khảo: Quan sát hiện tượng thí nghiệm: màu sắc của dung dịch trước và sau phản ứng.
Câu hỏi/Đề bài:
|
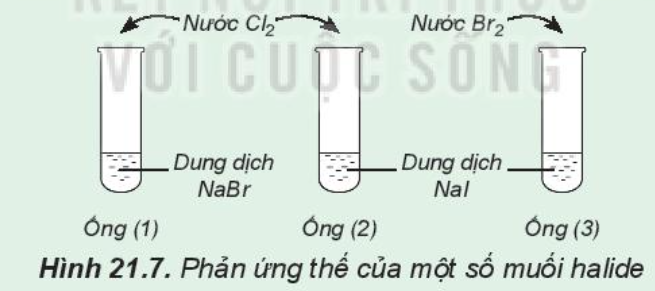
Phản ứng thế của một số muối halide Chuẩn bị: 3 ống nghiệm, dung dịch NaBr, dung dịch NaI, nước Cl2, nước Br2 loãng. Tiến hành: – Lấy khoảng 2 mL dung dịch NaBr vào ống nghiệm (1), 2 mL dung dịch NaI vào mỗi ống nghiệm (2) và (3) – Thêm vào ống nghiệm (1) và (2) vài giọt nước Cl2, thêm vào ống (3) vài giọt nước Br2, lắc đều các ống nghiệm Lưu ý: Cẩn thận không để nước Cl2, nước Br2 giây ra tay, quần áo Quan sát sự thay đổi màu của dung dịch trong các ống nghiệm và trả lời câu hỏi: 1. Nhận xét sự thay đổi màu của dung dịch trong các ống nghiệm 2. So sánh tính oxi hóa của Cl2, Br2, I2 3. Hãy chọn một thuốc thử để chứng tỏ có sự tạo thành I2 khi cho nước chlorine (hoặc nước bromine) tác dụng với dung dịch sodium iodine |
Hướng dẫn:
1. Quan sát hiện tượng thí nghiệm: màu sắc của dung dịch trước và sau phản ứng
2. Tính oxi hóa của Cl2 > Br2 > I2
3. Sử dụng hồ tinh bột để nhận biết I2
Lời giải:
1.
– Khi cho nước Cl2 vào dung dịch NaBr: dung dịch chuyển từ không màu thành màu vàng
– Khí cho nước Cl2 vào dung dịch NaI: dung dịch chuyển từ không màu thành màu vàng nâu
– Khi cho nước Br2 (màu vàng) vào dung dịch NaI: dung dịch chuyển từ không màu thành màu vàng nâu
2.
– Cl2 có thể oxi hóa ion Br– trong dung dịch NaBr thành Br2: Cl2 + NaBr → NaCl + Br2
=> Cl2 có tính oxi hóa mạnh hơn Br2
– Cl2 có thể oxi hóa ion I– trong dung dịch NaI thành I2: Cl2 + NaI → NaCl + I2
=> Cl2 có tính oxi hóa mạnh hơn I2
– Br2 có thể oxi hóa ion I– trong dung dịch NaI thành I2: Br2 + NaI → NaBr + I2
=> Br2 có tính oxi hóa mạnh hơn I2
=> Tính oxi hóa của Cl2 > Br2 > I2
3.
– Sử dụng thuốc thử là hồ tinh bột để chứng tỏ có sự tạo thành I2
=> Hiện tượng quan sát được: dung dịch màu vàng chuyển sang màu xanh tím