Trả lời Bài tập 1 Bài 14. Tính biến thiên enthalpy của phản ứng hóa học (trang 88, 89, 90, 91, 92, 93) – SGK Hóa 10 Chân trời sáng tạo. Tham khảo: Bước 1: Xác định số lượng liên kết và loại liên kết của các chất trong phản ứng.
Câu hỏi/Đề bài:
|
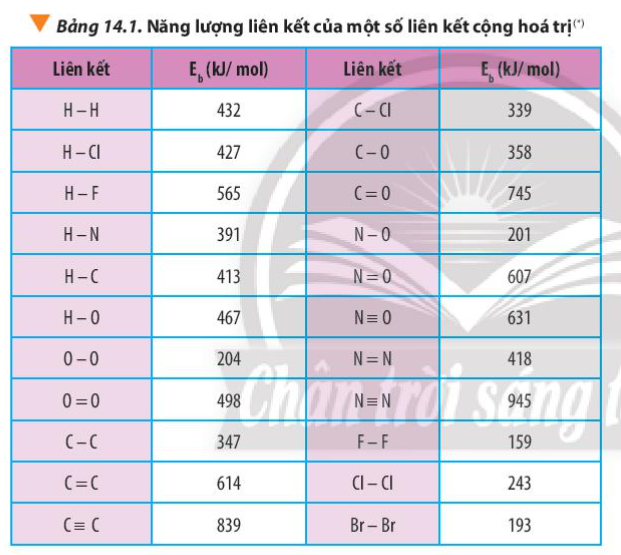
Bài 1: Tính \({\Delta _r}H_{298}^o\) của các phản ứng sau dựa theo năng lượng liên kết (sử dụng số liệu từ Bảng 14.1): a) N2H4(g) → N2(g) + 2H2(g) b) 4HCl(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2Cl2(g) + 2H2O(g) |
Hướng dẫn:
Bước 1: Xác định số lượng liên kết và loại liên kết của các chất trong phản ứng
Bước 2: Áp dụng công thức: \({\Delta _r}H_{298}^o\) = \(\Sigma \)Eb(cđ) – \(\Sigma \)Eb(sp)
Lời giải:
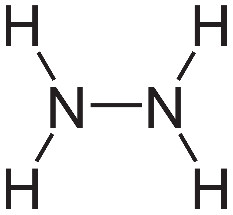
a) N2H4(g) → N2(g) + 2H2(g)
Công thức cấu tạo của N2H4:
\({\Delta _r}H_{298}^o\) = \(\Sigma \)Eb(cđ) – \(\Sigma \)Eb(sp)
=> \({\Delta _r}H_{298}^o\) = Eb(N2H4) – Eb(N2) – 2. Eb(H2)
= Eb(N-N) + 4.Eb(N-H) – Eb(N\( \equiv \)N) – 2.Eb(H-H)
=
b) 4HCl(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2Cl2(g) + 2H2O(g)
\({\Delta _r}H_{298}^o\) = \(\Sigma \)Eb(cđ) – \(\Sigma \)Eb(sp)
=> \({\Delta _r}H_{298}^o\) = 4.Eb(HCl) + Eb(O2) – 2.Eb(Cl2) – 2.Eb(H2O)
= 4.Eb(H-Cl) + Eb(O=O) – 2.Eb(Cl-Cl) – 2.2.Eb(O-H)
= 4.427 + 498 – 2.243 – 2.2.467 = -148 kJ