Lời giải Câu hỏi trang 71 Luyện tập Bài 13. Phản ứng oxi hóa – khử SGK Hóa 10 Cánh diều. Gợi ý: Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là điện tích của nguyên tử.
Câu hỏi/Đề bài:
|
1. Xác định số oxi hóa của mỗi nguyên tử nguyên tố trong các hợp chất ion Al2O3, CaF2. 2. Xác định số oxi hóa của mỗi nguyên tử trong hợp chất sau: N = O, CH4. |
Hướng dẫn:
– Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là điện tích của nguyên tử nguyên tố đó.
– Cách xác định số oxi hóa
+ Cách 1: Dựa theo số oxi hóa của một số nguyên tử đã biết.
Quy tắc 1. Trong các hợp chất: Số oxi hóa của H là +1 (trừ NaH, CaH2, …); Số oxi hóa của O là -2 (trừ OF2, H2O2, …); Số oxi hóa của các kim loại kiềm (nhóm IA: Li, Na, K, ..,) là +1, kim loại kiềm thổ (nhóm IIA: Be, Mg, Ca, Ba, …) là +2, số oxi hóa của Al là +3.
Quy tắc 2. Tổng các số oxi hóa của các nguyên tử trong phân tử bằng 0, của một ion đa nguyên tử bằng chính điện tích của ion đó.
+ Cách 2: Dựa theo công thức cấu tạo.
Cách tính điện tích các nguyên tử trong hợp chất với giả định đó là hợp chất ion dựa vào công thức cấu tạo.
Lời giải:
1.
– Al2O3: Số oxi hóa của O là -2.
Gọi a là số oxi hóa của Al. Áp dụng quy tắc 1 và 2
=> a.2 + (-2).3 = 0 → x = +3
Vậy số oxi hóa của O là -2, Al là +3
– CaF2
Gọi x là số oxi hóa của F, theo quy tắc 1 và 2 có:
1.(+2) + 2.x = 0 → x = -1.
Vậy số oxi hóa của Ca là +2, của F là -1.
2.
– N = O có công thức ion giả định là N2+O2-
Vậy số oxi hóa của N là +2, O là -2.
– CH4 có công thức ion giả định là C4-H4+
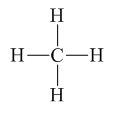
Vậy số oxi hóa của C là -4, H là +1.