Lời giải Bài tập 4 Bài 7. Xu hướng biến đổi một số tính chất của đơn chất – biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm (trang 38, 39, 40, 41, 42, 43, 44, 45) – SGK Hóa 10 Cánh diều.
Câu hỏi/Đề bài:
|
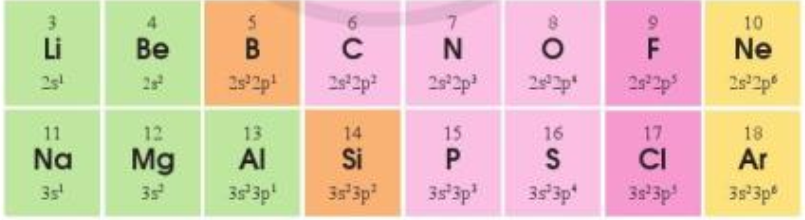
Bài 4: Cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 như sau:
b*) Giải thích vì sao sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3. Lấy một số ví dụ để minh họa sự biến đổi tính chất hóa học của đơn chất và hợp chất. |
Lời giải:
a)
– Ở chu kì 2: theo chiều tăng dần của điện tích hạt nhân
⟹ Số lớp electron ngoài cùng tăng từ 2s1 đến 2s22p6
– Ở chu kì 3: tương tự chu kì 2, theo chiều tăng dần của điện tích hạt nhân
⟹ Số lớp electron ngoài cùng tăng từ 3s1 đến 3s23p6
Vậy sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố ở chu kì 2 và 3 thể hiện như sau: đầu chu kì nguyên tố có cấu hình electron là ns1, cuối mỗi chu kì nguyên tố có cấu hình electron là ns2np6.
b*) – Sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3.
Vì cấu hình electron lớp ngoài cùng quyết định khả năng nhường và nhận e để đạt cấu hình của nguyên tố khí hiếm bền vững, dẫn tính kim loại hay phi kim của đơn chất. Trong 1 chu kì, theo chiều tăng của điện tích hạt nhân thì tính kim loại giảm dần, tính phi kim giảm dần.
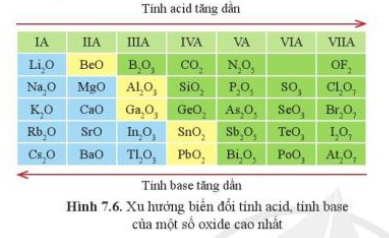
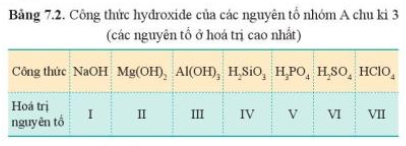
Từ đó, có sự biến đổi tuần hoàn tính acid, base của oxide cao nhất và hydroxide của các nguyên tố (ở hóa trị cao nhất) trong một chu kì.
 + Đơn chất: theo chiều tăng dần điện tích hạt nhân thì tính kim loại tăng dần từ và tính phi kim tăng dần (trừ Ar).- Ví dụ sự biến đổi tính chất hóa học của đơn chất và hợp chất của nguyên tố chu kì 3:
+ Đơn chất: theo chiều tăng dần điện tích hạt nhân thì tính kim loại tăng dần từ và tính phi kim tăng dần (trừ Ar).- Ví dụ sự biến đổi tính chất hóa học của đơn chất và hợp chất của nguyên tố chu kì 3:
Na chỉ cần nhường 1 electron để đạt cấu hình khí hiếm.
⟹ Na là kim loại mạnh nhất, có khả năng tác dụng với H2O ở điều kiện thường:
2Na + 2H2O → 2NaOH + H2
Mg chỉ tác dụng với H2O khi đun nóng:
Mg + 2H2O Mg(OH)2 + H2
+ Hợp chất: theo chiều tăng dần điện tích hạt nhân thì tính base của oxide và hydroxide giảm dần.
Na2O tan trong nước ở điều kiện thường tạo dung dịch base:
Na2O + H2O → 2NaOH
MgO và Al2O3 không tan được trong nước.
 a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố ở chu kì 2 và 3 thể hiện như thế nào?
a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố ở chu kì 2 và 3 thể hiện như thế nào?