Đáp án Bài tập 4 Bài 17. Nguyên tố và đơn chất halogen (trang 99, 100, 101, 102, 103, 104, 105, 106, 107, 108) – SGK Hóa 10 Cánh diều.
Câu hỏi/Đề bài:
|
Bài 4. Tra cứu các giá trị năng lượng liên kết ở phụ lục 2 a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của 2 phản ứng dưới đây: F2(g) + H2(g) → 2HF (g) O2(g) + 2H2(g) → 2H2O(g) b) Ở hai phản ứng trên, fluorine và oxygen đều đóng vai trò là chất oxi hóa. Dựa vào giá trị ∆rH0298, cho biết phản ứng oxi hóa – khử nào thuận lợi hơn |
Hướng dẫn:
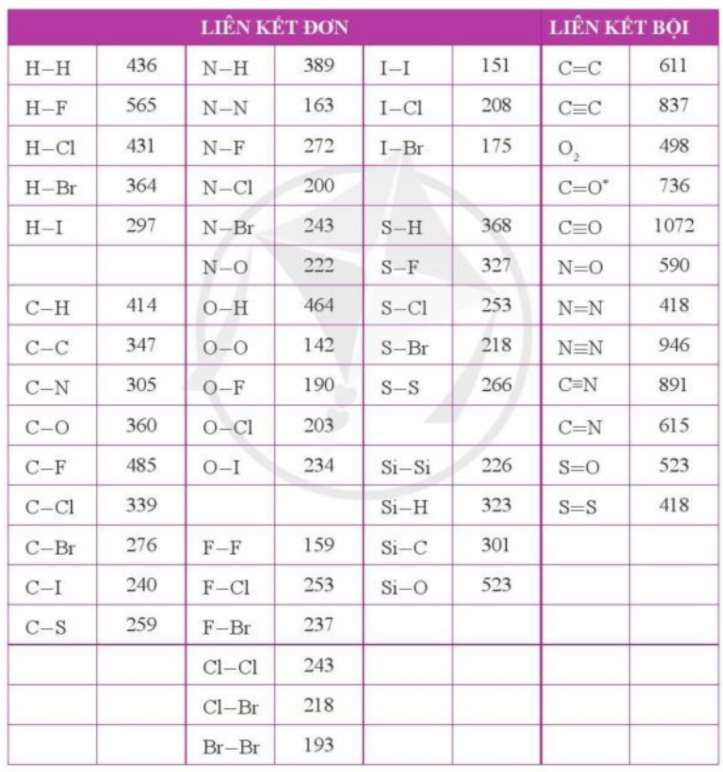
a)
∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF)
∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH)
b)
Giá trị biến thiên enthalpy nào âm hơn thì phản ứng đó diễn ra thuận lợi hơn
Lời giải:
a)
– Xét phản ứng: F2(g) + H2(g) → 2HF (g)
+ Ta có: ∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF) = 159 + 436 – 2×565 = -535 (kJ/mol)
– Xét phản ứng: O2(g) + 2H2(g) → 2H2O(g)
+ Ta có: ∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH) = 142 + 2×436 – 2x2x464 = -842 (kJ/mol)
b)
Giá trị biến thiên enthalpy của phản ứng (2) âm hơn giá trị biến thiên enthalpy của phản ứng (1)
=> Phản ứng oxi hóa – khử (2) diễn ra thuận lợi hơn