Giải Bài tập 3 Bài 10. Liên kết ion (trang 53, 54, 55, 56) – SGK Hóa 10 Cánh diều. Hướng dẫn: Vẽ sơ đồ nguyên tử Na, Mg nhường electron ở lớp vỏ ngoài cùng.
Câu hỏi/Đề bài:
|
Bài 3: a) Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng b) Vì sao cả Na2O và MgO đều là chất rắn ở nhiệt độ thường? c) Vì sao nhiệt độ nóng chảy của MgO (2 852oC) cao hơn rất nhiều so với Na2O (1 132oC)? |
Hướng dẫn:
a) Vẽ sơ đồ nguyên tử Na, Mg nhường electron ở lớp vỏ ngoài cùng
b) Na2O và MgO là hợp chất ion
c) Dựa vào năng lượng phân li.
Lời giải:
a)
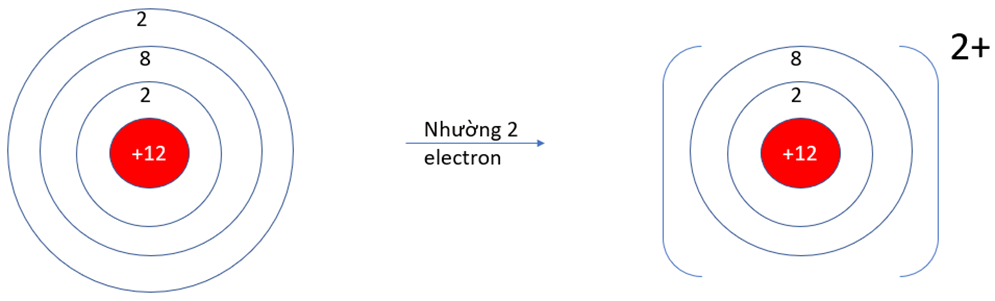
– Ở dạng nguyên tử, Na và Mg đều có 3 lớp electron. Ở dạng ion Na+, Mg2+ chỉ có 2 lớp electron
=> Bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b, Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion nên ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion nên ở điều kiện thường MgO tồn tại ở thể rắn.
c, Tá có:
+ Bán kính ion Na+ < bán kính ion Mg2+.
+ Điện tích ion Mg2+ < điện tích ion Na+.
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.